การจัดเรียงอิเล็กตรอน: พื้นฐานแห่งความเข้าใจธาตุ
คำนำ
การจัดเรียงอิเล็กตรอนเป็นแนวคิดพื้นฐานในวิชาเคมีที่ช่วยอธิบายพฤติกรรมและสมบัติของธาตุต่างๆ ทั้งนี้ การจัดเรียงอิเล็กตรอนของธาตุนั้นจะกำหนดคุณสมบัติทางเคมี เช่น ความสามารถในการทำปฏิกิริยา ความเป็นโลหะ และความเป็นอโลหะ บทความนี้จะให้ข้อมูลเชิงลึกเกี่ยวกับการจัดเรียงอิเล็กตรอน รวมถึงความสำคัญและวิธีการคาดการณ์การจัดเรียงอิเล็กตรอน
หลักการพื้นฐานของการจัดเรียงอิเล็กตรอน
อะตอมประกอบด้วยโปรตอน นิวตรอน และอิเล็กตรอน ซึ่งอิเล็กตรอนเป็นอนุภาคที่มีประจุลบและโคจรอยู่รอบนิวเคลียสของอะตอม นิวเคลียสซึ่งประกอบด้วยโปรตอนและนิวตรอน มีประจุบวกและเป็นส่วนกลางของอะตอม
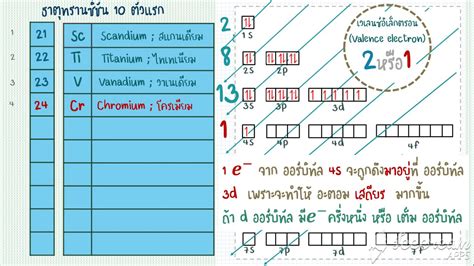
อิเล็กตรอนในอะตอมถูกจัดเรียงอยู่ในระดับพลังงานที่แตกต่างกัน ระดับพลังงาน เป็นชั้นที่อิเล็กตรอนโคจรอยู่รอบนิวเคลียส แต่ละระดับพลังงาน สามารถรองรับอิเล็กตรอนได้จำนวนจำกัด โดยระดับพลังงานที่อยู่ใกล้กับนิวเคลียสมากที่สุดจะมีพลังงานต่ำที่สุด และระดับพลังงานที่อยู่ห่างจากนิวเคลียสมากที่สุดจะมีพลังงานสูงที่สุด

การเขียนการจัดเรียงอิเล็กตรอน
การเขียนการจัดเรียงอิเล็กตรอนแสดงให้เห็นจำนวนอิเล็กตรอนในแต่ละระดับพลังงานของอะตอมโดยใช้ตัวเลขหรือตัวอักษร ตัวอย่างเช่น การจัดเรียงอิเล็กตรอนของอะตอมไฮโดรเจนเขียนเป็น 1s¹ ซึ่งหมายความว่าอะตอมไฮโดรเจนมีอิเล็กตรอนหนึ่งตัวในระดับพลังงานที่ใกล้เคียงกับนิวเคลียสซึ่งกำหนดให้เป็น 1s
ระดับพลังงานแต่ละระดับจะถูกแบ่งออกเป็น ออร์บิทัล ซึ่งเป็นพื้นที่ที่อิเล็กตรอนมีแนวโน้มอยู่มากที่สุด ออร์บิทัลมีรูปร่างที่แตกต่างกัน ซึ่งแต่ละออร์บิทัลสามารถรองรับอิเล็กตรอนได้สูงสุดสองตัวที่มีสปินตรงข้ามกัน
หลักการกีดกันของเพาลี
หลักการกีดกันของเพาลีระบุว่าอิเล็กตรอนสองตัวในอะตอมเดียวกันไม่สามารถมีชุดตัวเลขควอนตัมเหมือนกันได้ ชุดตัวเลขควอนตัมเป็นชุดของตัวเลขที่อธิบายสถานะของอิเล็กตรอน ซึ่งรวมถึงระดับพลังงาน หมายเลขควอนตัมของโมเมนตัมเชิงมุม และหมายเลขควอนตัมของสปิน
หลักการ Aufbau
หลักการ Aufbau ใช้เพื่อคาดการณ์การจัดเรียงอิเล็กตรอนของอะตอม โดยระบุว่าอิเล็กตรอนจะเติมระดับพลังงานและออร์บิทัลที่มีพลังงานต่ำที่สุดก่อน

ตารางการจัดเรียงอิเล็กตรอน
ตารางการจัดเรียงอิเล็กตรอนแสดงลำดับของระดับพลังงาน ออร์บิทัล และจำนวนอิเล็กตรอนสูงสุดที่สามารถอยู่ในแต่ละออร์บิทัล
| ระดับพลังงาน |
ออร์บิทัล |
จำนวนอิเล็กตรอนสูงสุด |
| n=1 |
1s |
2 |
| n=2 |
2s |
2 |
| n=3 |
3s |
2 |
| n=4 |
4s |
2 |
| n=5 |
5s |
2 |
| n=6 |
6s |
2 |
| n=7 |
7s |
2 |
ความสำคัญของการจัดเรียงอิเล็กตรอน
การจัดเรียงอิเล็กตรอนเป็นสิ่งสำคัญเนื่องจากช่วยอธิบายสมบัติทางเคมีของธาตุ ได้แก่:
-
ความสามารถในการทำปฏิกิริยา: จำนวนอิเล็กตรอนในระดับพลังงานชั้นนอกสุดของอะตอมจะกำหนดความสามารถในการทำปฏิกิริยา โดยทั่วไปแล้ว ธาตุที่มีอิเล็กตรอนในระดับพลังงานชั้นนอกสุดมากหรือมีอิเล็กตรอนเพียงเล็กน้อยจะมีความสามารถในการทำปฏิกิริยาสูง
-
ความเป็นโลหะและความเป็นอโลหะ: ธาตุที่มีอิเล็กตรอนในระดับพลังงานชั้นนอกสุดมากมักจะเป็นโลหะ ส่วนธาตุที่มีอิเล็กตรอนในระดับพลังงานชั้นนอกสุดน้อยมักจะเป็นอโลหะ
-
สมบัติทางเคมีอื่นๆ: การจัดเรียงอิเล็กตรอนยังมีส่วนทำให้เกิดสมบัติทางเคมีอื่นๆ เช่น จุดหลอมเหลว จุดเดือด ความหนาแน่น และโครงสร้างทางผลึก
วิธีการคาดการณ์การจัดเรียงอิเล็กตรอน
การจัดเรียงอิเล็กตรอนของอะตอมใดๆ สามารถคาดการณ์ได้จากเลขอะตอมของอะตอม เลขอะตอมแสดงถึงจำนวนโปรตอนในอะตอม ซึ่งสอดคล้องกับจำนวนอิเล็กตรอนในอะตอมที่เป็นกลางทางไฟฟ้า
ขั้นตอนในการคาดการณ์การจัดเรียงอิเล็กตรอน:
- เขียนเลขอะตอมของอะตอม
- ใช้หลักการ Aufbau เพื่อเติมอิเล็กตรอนในระดับพลังงานและออร์บิทัลที่มีพลังงานต่ำที่สุดก่อน
- ตรวจสอบให้แน่ใจว่าออร์บิทัลทั้งหมดมีอิเล็กตรอนสูงสุดสองตัวที่มีสปินตรงข้ามกันตามหลักการกีดกันของเพาลี
- เขียนการจัดเรียงอิเล็กตรอนของอะตอมโดยใช้ตัวเลขหรือตัวอักษร
การประยุกต์ใช้ของการจัดเรียงอิเล็กตรอน
การจัดเรียงอิเล็กตรอนมีการประยุกต์ใช้ในสาขาต่างๆ ของวิทยาศาสตร์ รวมถึง:
-
เคมี: การจัดเรียงอิเล็กตรอนช่วยในการทำความเข้าใจการเกิดพันธะเคมี ปฏิกิริยาเคมี และสมบัติของสารประกอบ
-
ฟิสิกส์: การจัดเรียงอิเล็กตรอนมีส่วนช่วยในการทำความเข้าใจสมบัติทางไฟฟ้าและแม่เหล็กของวัสดุ
-
วัสดุศาสตร์: การจัดเรียงอิเล็กตรอนใช้ในการออกแบบและพัฒนาวัสดุที่มีสมบัติเฉพาะ
สรุป
การจัดเรียงอิเล็กตรอนเป็นแนวคิดพื้นฐานที่ช่วยอธิบายสมบัติทางเคมีและสมบัติอื่นๆ ของธาตุ การทำความเข้าใจการจัดเรียงอิเล็กตรอนมีความสำคัญอย่างยิ่งในสาขาต่างๆ ของวิทยาศาสตร์และมีการประยุกต์ใช้ในด้านต่างๆ เช่น การออกแบบยา การพัฒนาวัสดุ และการทำความเข้าใจกระบวนการทางชีวเคมี

